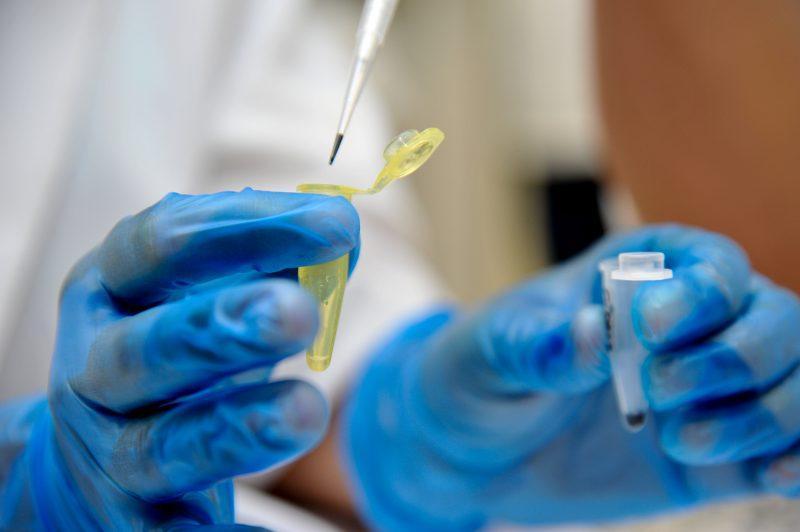
São Paulo – A Agência Nacional de Vigilância Sanitária (Anvisa) suspendeu os estudos clínicos com CoronaVac – vacina que está sendo desenvolvida pela empresa chinesa Sinovac em parceria com o Instituto Butantan – depois de um “evento adverso grave” em uma das pessoas submetidas aos testes. Com a interrupção do estudo, nenhum novo voluntário poderá ser vacinado.
“O evento ocorrido no dia 29 de outubro comunicado à Agência, que decidiu interromper o estudo para avaliar os dados observados até o momento e julgar o risco/benefício da continuidade do estudo”, disse a Anvisa num comunicado publicado ontem à noite.
A interrupção dos estudos por causa de evento adverso grave está prevista nas normas da Anvisa e aconteceu também com outras vacinas contra a covid-19 que estão em fase de testes – a da Janssen, em 12 de outubro, e a da Universidade de Oxford e da AstraZeneca, em 9 de setembro.
O evento adverso grave é caracterizado por óbito, efeito adverso potencialmente fatal, invalidez persistente ou significativa, internação hospitalar ou prolongamento de internação, anomalia congênita ou defeito de nascimento, suspeita de transmissão de agente infeccioso ou outro evento clinicamente significante.
Em nota, a Sinovac disse que conversou com o Instituto Butantan e que a instituição “acredita que o evento adverso grave não está relacionado à vacina”.
Ontem, em entrevista ao Jornal da Cultura, o diretor do Instituto Butantan, Dimas Covas, disse que uma das pessoas que participou dos testes com a CoronaVac morreu em outubro, mas que a morte não estava relacionada à vacina.
“A Anvisa foi notificada de um óbito, não de efeito adverso. Até estranhamos um pouco essa decisão da Anvisa porque é um óbito não relacionado à vacina”, disse ele. “São mais de 10 mil voluntários neste momento, pode acontecer óbito. O sujeito pode ter acidente de trânsito e morrer”, afirmou.
IMPORTAÇÃO DE DOSES
Ontem, o governador do estado de São Paulo, João Doria, anunciou que doses da CoronaVac vacina começarão a chegar ao Brasil no próximo dia 20. A vacinação, porém, só começará depois que houver autorização da Anvisa.
“As primeiras 120 mil doses chegam em 20 de novembro no Aeroporto Internacional de Guarulhos. Virão em lotes e até 30 de dezembro teremos 6 milhões de vacinas aqui em São Paulo”, disse Doria durante um pronunciamento.
Ele acrescentou que, além destas doses, também devem ser importados os insumos das vacinas, o que permitirá a produção de 40 milhões de doses adicionais. Os insumos para 1,2 milhão de vacinas chegarão ao Brasil até 27 de novembro, e até janeiro devem ser enviados materiais suficientes para a produção das outras 38,8 milhões de doses.
Doria afirmou também que em 2 de novembro começaram as obras da nova fábrica de vacinas do Instituto Butantan e que as instalações ficarão prontas em setembro de 2021. Quando concluída, a fábrica poderá produzir 100 milhões de doses da vacina contra covid-19 por ano.
A produção das vacinas contra a covid-19 a partir dos insumos que serão importados até o início do ano que vem independe da conclusão das obras da nova fábrica do Instituto Butantan.
“O Butantan detém essa tecnologia”, disse o diretor do Instituto, Dimas Covas, durante uma entrevista coletiva. “[Se o insumo] chega hoje dá para começar depois de amanhã. Estamos aptos a fazer até 1 milhão de doses por dia”, acrescentou.