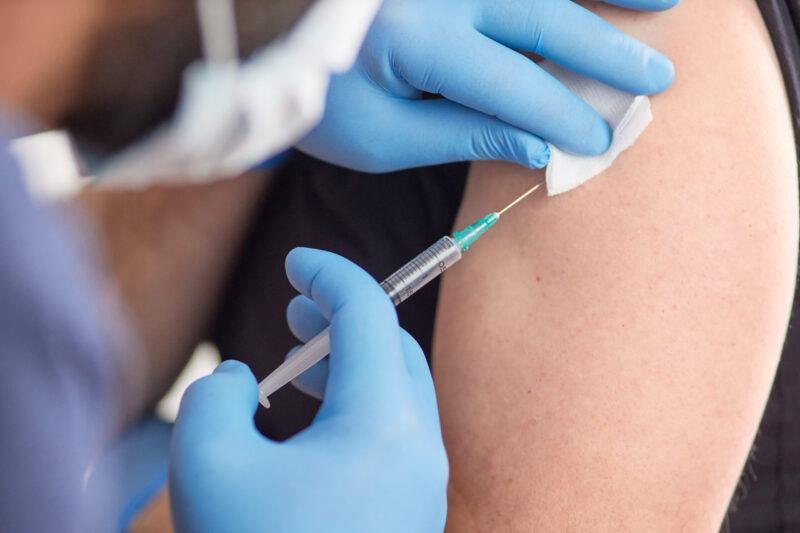
São Paulo – A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou ontem por unanimidade o uso emergencial das vacinas contra a covid-19 desenvolvidas pela Sinovac e pela AstraZeneca no Brasil. Elas serão produzidas aqui respectivamente pelo Instituto Butantan e pela Fundação Oswaldo Cruz (Fiocruz).
A autorização da agência é para a aplicação de aproximadamente 6 milhões de doses da vacina da Sinovac, que já estão em solo brasileiro, e de 2 milhões de doses do imunizante da Astrazeneca, que deveriam ter sido trazidas no final de semana mas tiveram a exportação bloqueada pela India, país onde foram produzidas. Segundo o Ministério da Saúde, estas doses devem chegar ao Brasil ainda esta semana.
O uso de outras doses das mesmas vacinas terá de passar pelo crivo da Anvisa novamente, seja por meio do protocolo de avaliação de uso emergencial, seja por meio do pedido de registro definitivo das vacinas – que na prática serve como autorização definitiva para o uso dos imunizantes.
No voto a favor do uso emergencial das vacinas, a relatora do caso e diretora da Anvisa, Meiruze Sousa Freitas, destacou o efeito negativo da covid-19 no Brasil – “o nosso País atualmente responde por 10% do total das mortes observadas no mundo” – e rebateu a alegação do presidente Jair Bolsonaro e do ministro da Saúde, Eduardo Pazuello, de que a doença é tratável com medicamentos – algo que o governo convencionou chamar de “tratamento precoce”.
“Até o momento, não contamos com alternava terapêutica, aprovada e disponível para prevenir ou tratar a doença causada pelo novo coronavírus. Assim, compete a cada um de nós, instituições públicas e privadas, sociedade civil organizada e cidadãos, cada um na sua esfera de atuação, tomarmos todas as medidas ao nosso alcance para, no menor tempo possível, diminuirmos o impacto devastador da covid-19 sobre as vidas do nosso país”, afirmou.
TERMO DE COMPROMISSO
O uso emergencial da vacina da Sinovac foi aprovado sob a condição de que o Instituto Butantan apresente informações complementares quanto à chamada imunogenicidade da substância – a capacidade da vacina incentivar o organismo a produzir anticorpos contra o agente causador da doença.
Segundo Freitas, o Butantan ainda precisa mostrar a quantidade de anticorpos gerados nas amostras dos voluntários participantes dos estudos. Sem isso, diz a agência, é inviável determinar por quanto tempo dura a proteção conferida pela vacina.
“Esse documento, portanto, deve complementar as informações referentes à imunidade conferida aos voluntários que receberam a vacina na terceira fase de desenvolvimento clínico. O dado é imprescindível para que se possa concluir a duração da resposta imunológica nos indivíduos vacinados”, disse ela em seu parecer.
O Instituto Butantan terá que entregar esta informação complementar à Anvisa até dia 28 de fevereiro. O diretor do instituto, Dimas Covas, disse em entrevista coletiva ontem que já assinou o termo de compromisso e que os dados serão enviados à Anvisa.